Phoxilium 1.2 Mmol/L Phosphate Solution For Haemodialysis/ Haemofiltration
phq (jlium
UK, IE, MT Package leaflet: Information for the user.............................3
PT Folheto informativo: Informafao para o utilizador...............6
ES Prospecto: Informacion para el usuario...............................9
UK, IE, MT The following information is intended
for healthcare professionals only.......................................12
PT A informa?ao que se segue destina-se
apenas aos profissionais de saude...................................14
ES Esta informacion esta destinada
unicamente a profesionales del sector sanitario...............16
THIS PAGE IS INTENTIONALLY LEFT BLANK
Package leaflet: Information for the user
UK IE MT
PHOXILIUM 1.2 mmol/l phosphate
Solution for haemodialysis and haemofiltration
Calcium chloride dihydrate, magnesium chloride hexahydrate, sodium chloride, sodium hydrogen carbonate, potassium chloride, disodium phosphate dihydrate Read all of this leaflet carefully before you start using this medicine because it contains important information for you.
• Keep this leaflet. You may need to read it again.
• If you have any further questions, ask your doctor or pharmacist or nurse.
• If you get any side effects, talk to your doctor or pharmacist or nurse. This includes any possible side effects not listed in this leaflet. See section 4.
WHAT IS IN THIS LEAFLET:
1. What PHOXILIUM is and what it is used for
2. What you need to know before you are given PHOXILIUM
3. How to use PHOXILIUM
4. Possible side effects
5. How to store PHOXILIUM
6. Contents of the pack and other information
1. WHAT PHOXILIUM IS AND WHAT IT IS USED FOR
PHOXILIUM, belonging to the group of hemofiltrates solution, contains calcium chloride dihydrate, magnesium chloride hexahydrate, sodium chloride, sodium hydrogen carbonate, potassium chloride, disodium phosphate dihydrate. PHOXILIUM is used in hospitals in intensive care treatments to correct chemical imbalance of the blood which is caused by kidney injury. The treatments, using continuous renal replacement therapy, are designed to remove accumulated waste products from the blood when the kidneys are not functioning.
The PHOXILIUM solution is
particularly used to treat critically ill patients with acute kidney injury having:
• a normal concentration of potassium in the blood (normal kalaemia) or
• a normal or low concentration of phosphate in the blood (normal or hypophosphataemia).
2. WHAT YOU NEED TO KNOW BEFORE YOU ARE GIVEN PHOXILIUM
DO NOT USE PHOXILIUM ON PATIENTS WITH ANY OF THE FOLLOWING THREE CONDITIONS:
• a high concentration of potassium in the blood (hyperkalae-mia)
• a high concentration of bicarbonate in the blood (metabolic alkalosis)
• a high concentration of phosphate in the blood (hyperphos-phataemia)
DO NOT USE HAEMODIALYSIS OR HAEMOFILTRATION IN ANY OF THE FOLLOWING THREE CASES:
• when haemofiltration cannot correct the symptoms caused by a high blood concentration of urea (uraemic symptoms) which are the result of renal injury with pronounced hypercatabolism (an abnormally increased process of breaking down substances),
• insufficient arterial pressure in the access to the blood vessel,
• reduced clotting of the blood (systemic anticoagulation), if there is a high risk of bleeding.
WARNINGS AND PRECAUTIONS
Talk to your doctor or pharmacist or nurse before you are using PHOXILIUM.
Before and during treatment, your blood condition will be checked, e.g. your acid-base balance and concentrations of salts in the blood (electrolytes) will be monitored, including all fluid inputs (intravenous infusion) and outputs (urine output), even those not directly related to CRRT.
OTHER MEDICINES AND PHLOXILIUM
Tell your doctor or pharmacist if you are using, have recently used or might use any other medicines. This is because the concentration of other medicines may influence the treatment with PhOxILIUM. Your doctor will decide if any changes in the dosage of your medicines should be made.
In particular, tell your doctor if you are using either of the following:
• Additional sources of phosphate (e.g. nutritional fluids); as this may increase the risk of a high concentration of phosphate in the blood (hyperphosphatemia).
• Vitamin D and medicinal products containing calcium chloride or calcium gluconate; as they can increase the risk of a high concentration of calcium in the blood (hypercalcaemia).
• Sodium bicarbonate; as this may increase the risk of excess of bicarbonate in your blood (metabolic alkalosis).
PREGNANCY, BREAST-FEEDING AND FERTILITY
Pregnancy and breast-feeding: There is no documented clinical data on the use of this medicine during pregnancy and lactation. This medicine should only be administered to pregnant and lactat-ing women if clearly needed. Fertility:
No effects on fertility are anticipated, since calcium, sodium, potassium, magnesium, chloride, hydrogen phosphate and hydrogen carbonate are normal constituents of the body.
DRIVING AND USING MACHINES
PHOXILIUM will not have any effect on the ability to drive or use machines.
3. HOW TO USE PHOXILIUM
PHOXILIUM is a product to be used in hospitals and administered by medical professionals only. The volume of PHOXILIUM, and therefore the dose, used will depend on your condition. The dose volume will be determined by the physician responsible for your treatment.
|
composition is: |
mmol/l |
|
Calcium, Ca2+ |
1.25 |
|
Magnesium, Mg2+ |
0.6 |
|
Sodium, Na+ |
140 |
|
Chloride, Cl- |
115.9 |
|
Hydrogen phosphate, HPO42- |
1.2 |
|
Hydrogen carbonate, HCO3- |
30 |
|
Potassium, K+ |
4 |
|
Theoretical Osmolarity: | |
|
293 mOsm/l | |
|
The other ingredients are: |
PHOXILIUM can be administered directly into the bloodstream (Intravenously) or via haemodialysis, where the solution flows on one side of a dialysis membrane while the blood flows on the other side. Always use this medicine exactly as your doctor, pharmacist or nurse has told you. Check with your doctor, pharmacist or nurse if you are not sure.
For instructions for use, please see section “The following information is intended for healthcare professionals only”.
IF YOU USE MORE PHOXILIUM THAN YOU SHOULD
PHOXILIUM is a product to be used in hospitals and administered by medical professionals only and your fluid balance and blood chemistry will be carefully monitored.
THEREFORE IT IS UNLIKELY THAT YOU WILL USE MORE PHOXILIUM THAN YOU SHOULD.
In the unlikely event that an overdose occurs, your doctor will take the necessary corrective measures and adjust your dose.
Overdose may result in fluid overload, reduction of the plasma bicarbonate concentration (metabolic acidosis) and/or high phosphate concentration (hyperphosphatae-mia) if you are suffering from renal injury.
It could lead to severe consequences, such as congestive heart failure or disturbances in your blood chemistry.
If you have any further questions on the use of this product, please ask your doctor or pharmacist.
4. POSSIBLE SIDE EFFECTS
Like all medicines, this medicine can cause side effects, although not everybody gets them.
The following three side effects related to the use of PHOXILIUM are possible:
• abnormally high or low volume of water in the body (hyper or hypovolaemia),
• changes in levels of salt in the blood (electrolyte imbalance such as hyperphosphataemia)
• elevation of the plasma bicarbonate concentration (metabolic alkalosis) or reduction of the plasma bicarbonate concentration (metabolic acidosis).
There are also some side effects which can be caused by dialysis treatments, such as:
• nausea, vomiting, muscle cramps and low blood pressure (hypotension).
REPORTING OF SIDE EFFECTS
If you get any side effects, talk to your doctor or pharmacist or nurse. This includes any possible side effects not listed in this leaflet.
You can also report side effects directly via:
Malta
ADR Reporting
Website: www.medicinesauthority. gov.mt/adrportal
Republic of Ireland
HPRA Pharmacovigilance,
Earlsfort Terrace, IRE - Dublin 2. Tel: +353 1 6764971,
Fax: +353 1 6762517,
Website: www.hpra.ie;
E-mail: medsafety@hpra.ie UK
Yellow Card Scheme www.mhra.gov.uk/yellowcard
By reporting side effects you can help provide more information on the safety of this medicine.
5. HOW TO STORE PHOXILIUM
Keep this medicine out of the sight and reach of children.
Do not use this medicine after the expiry date which is stated on the label and the packaging. The expiry date refers to the last day of that month.
Store between +4° - +30°C. Do not refrigerate or freeze.
Chemical and physical in-use stability of the reconstituted solution has been demonstrated for 24 hours at 22°C. If not used immediately in-use storage times and conditions prior to use are the responsibility of the user and should not be longer than 24 hours including the duration of the treatment.
Do not use this medicine if the solution is cloudy or the overwrap is damaged. All seals must be intact. Do not throw away any medicines via wastewater or household waste. Ask your pharmacist how to throw away medicines you no longer use. These measures will help protect the environment.
6. CONTENTS OF THE PACK AND OTHER INFORMATION
WHAT PHOXILIUM CONTAINS
The active substances before and after mixing (reconstitution) are shown below.
Active substances before mixing:
1000 ml of solution from the small compartment (A) contains:
Calcium chloride, 2 H2O 3.68 g Magnesium chloride, 6 H2O 2.44 g
1000 ml of solution from the large compartment (B) contains:
Sodium hydrogen carbonate 2.92 g Potassium chloride 0.314 g
Disodium
Active substances after mixing:
The solutions in the compartments A (250 ml) and B (4750 ml) are mixed to give one reconstituted solution (5000 ml) of which the
• carbon dioxide (for pH adjustment) E290,
• hydrochloric acid (for pH adjustment) E507 and
• water for injections.
WHAT PHOXILIUM LOOKS LIKE AND CONTENTS OF THE PACK
PHOXILIUM is a solution for haemodialysis and haemofiltration presented in a two compartment bag. The final reconstituted solution is obtained after breaking the peel seal and mixing both solutions.
The reconstituted solution is clear and colourless. Each bag (A+B) contains 5000 ml solution for haemodialysis and haemofiltration. The bag is overwrapped with a transparent film.
Each box contains two bags and one package leaflet.
MARKETING AUTHORISATION HOLDER:
Gambro Lundia AB Magistratsvagen 16 SE-226 43 Lund Sweden
MANUFACTURER:
Gambro Dasco S.p.A.
Sondalo Plant Via Stelvio 94 23035 Sondalo (SO)
Italy
This medicinal product is authorised in the Member States of the EEA under the following names:
Austria, Belgium, Bulgaria, Cyprus, Denmark, Estonia, Finland, France, Germany, Greece, Iceland, Ireland, Italy, Latvia, Lithuania, Luxembourg, Malta, the Netherlands, Norway, Poland, Portugal, Romania, Slovakia, Slovenia, Spain, Sweden, United Kingdom: PHOXILIUM
Hungary: PHOXIL
This leaflet was last revised in 07/2016
PHOXILIUM® 1,2 mmol/l fosfato Solugao para hemodialise ou hemofiltragao
Cloreto de calcio di-hidratado, cloreto de magnesio hexa-hidratado, cloreto de sodio, bicarbonato de sodio, cloreto de potassio, fosfato dissodico di-hidratado
Leia com atengao todo este folheto antes de comegar a utilizar este medicamento, pois contem informagao importante para si.
• Conserve este folheto. Pode ter necessidade de o ler novamente.
• Caso ainda tenha duvidas, fale com o seu medico, farmaceutico ou enfermeiro.
• Se tiver quaisquer efeitos secundarios, incluindo possiveis efeitos secundarios nao indicados neste folheto, fale com o seu medico, farmaceutico ou enfermeiro. Ver secgao 4.
O que contem este folheto:
1. O que e Phoxilium e para que e utilizado
2. O que precisa de saber antes de receber Phoxilium
3. Como utilizar Phoxilium
4. Efeitos secundarios possiveis
5. Como conservar Phoxilium
6. Conteudo da embalagem e outras informagoes
1. O que e Phoxilium e para que e utilizado_
O Phoxilium, pertencendo ao grupo das solugoes para hemofiltragao, contem cloreto de calcio di-hidratado, cloreto de magnesio hexa-hidratado, cloreto de sodio, bicarbonato de sodio, cloreto de potassio e fosfato dissodico di-hidratado.
O Phoxilium e utilizado em tratamen-tos de cuidados intensivos a nivel hos-pitalar para corregao de desequilibrios quimicos no sangue provocados pela lesao renal.
Os tratamentos que utilizam a tera-peutica de substituigao renal continua foram concebidos para remover os residuos acumulados no sangue quando os rins nao funcionam.
A solugao Phoxilium e utilizada especificamente para o tratamento de doentes em estado critico com lesao renal aguda que apresentem:
• uma concentragao normal de potassio no sangue (caliemia normal) ou
• uma concentragao normal ou reduzida de fosfato no sangue (fosfatemia normal ou hipofosfa-temia).
2. O que precisa de saber antes de receber Phoxilium_
Nao utilize Phoxilium em doentes que apresentem alguma das tres condigoes que se seguem:
• uma elevada concentragao de potassio no sangue (hipercaliemia)
• uma elevada concentragao de bicarbonato no sangue (alcalose metabolica)
• uma elevada concentragao de fos-fato no sangue (hiperfosfatemia)
Nao recorra a hemodialise ou a hemofiltragao em nenhum dos tres casos que se seguem:
• quando a hemofiltragao e incapaz de corrigir os sintomas causados por uma concentragao elevada de ureia no sangue (sintomas uremi-cos) que resultam da lesao renal com hipercatabolismo acentuado (um processo de degradagao
de substancias anormalmente aumentado).
• pressao arterial insuficiente no acesso vascular,
• coagulagao sanguinea reduzi-da (anticoagulagao sistemica), caso exista um risco elevado de hemorragia.
Advertencias e precaugoes
Fale com o seu medico, farmaceu-tico ou enfermeiro antes de utilizar Phoxilium.
Antes e durante o tratamento, os seus parametros sanguineos serao monitorizados, por ex., o equiHbrio acido-base e as concentragoes san-guineas de sais minerais (eletrolitos) serao monitorizados, incluindo todos os aportes (perfusao intravenosa) e perdas (saida de urina) de fluidos, mesmo os que nao estao diretamente relacionados com CRRT.
Outros medicamentos e Phoxilium
Informe o seu medico ou farmaceutico se estiver a utilizar, ou tiver utilizado recentemente, ou se vier a utilizar outros medicamentos. Isto porque a concentragao sanguinea de outros medicamentos podera influenciar o tratamento com Phoxilium. O seu medico decidira se a dosagem dos seus medicamentos deve ser alterada. Informe o seu medico, particular-mente, no caso de estar a utilizar os seguintes:
• Fontes adicionais de fosfato (por ex., fluidos nutricionais), visto que pode aumentar o risco de concentragoes elevadas de fosfato no sangue (hiperfosfatemia).
• Vitamina D e medicamentos que contenham cloreto de calcio ou gluconato de calcio, visto que podem aumentar o risco de uma concentragao elevada de calcio no sangue (hipercalcemia).
• Bicarbonato de sodio, visto que pode aumentar o risco de excesso de bicarbonato no sangue (alcalo-se metabolica).
Gravidez, amamentagao e fertilidade
Gravidez e amamentagao:
Nao existem dados clinicos docu-mentados sobre a utilizagao deste medicamento durante a gravidez e a amamentagao. Este medicamento apenas devera ser administrado a gravidas e mulheres durante o periodo de amamentagao se for estritamente necessario.
Fertilidade:
Nao estao previstos quaisquer efeitos na fertilidade, pois o calcio, o sodio, o potassio, o magnesio, o cloreto, o hidrogenofosfato e o bicarbonato sao constituintes normais do corpo.
Condugao de veiculos e utilizagao de maquinas
O Phoxilium nao tem qualquer efeito sobre a capacidade de condugao de veiculos ou de utilizagao de maquinas.
Qual a composipao de Phoxilium
As substancias ativas antes e apos a mistura (reconstituipao) estao abaixo indicadas.
Substancias ativas antes da mistura:
1000 ml de solupao no compartimen-
3. Como utilizar Phoxilium
O Phoxilium e um produto a ser utilizado a nivel hospitalar e a ser administrado unicamente por pessoal medico. O volume de Phoxilium e, consequentemente, a dose utilizada, depende da condipao do doente. O volume da dose fica ao criterio do medico responsavel pelo tratamento.
O Phoxilium pode ser administrado diretamente na circulapao sanguinea (via intravenosa) ou por hemodialise, com a solupao a fluir de um lado de uma membrana de dialise e o sangue a fluir no outro lado.
Utilize este medicamento exatamente de acordo com as indicapoes do seu medico, farmaceutico ou enfermeiro. Fale com o seu medico, farmaceutico ou enfermeiro se tiver duvidas.
Para obter instrupoes de utilizapao, consulte a secpao “A seguinte informa-pao e dirigida apenas aos profissionais de saude”.
Se utilizar mais Phoxilium do que deveria
O Phoxilium e um produto a ser utilizado a nivel hospitalar e a ser administrado unicamente por pessoal medico. O seu equilibrio hidrico e os seus parametros quimicos sanguineos serao cuidadosamente monitorizados.
Consequentemente, o uso excessivo de Phoxilium e improvavel.
No caso improvavel de sobredo-sagem, o seu medico ira tomar as medidas corretivas necessarias e ajustar a dose.
A sobredosagem podera resultar numa sobrecarga hidrica, redupao da concentrapao de bicarbonato no plasma (acidose metabolica) e/ ou concentrapao elevada de fosfato (hiperfosfatemia) se o doente sofrer de lesao renal. Podera ter consequencias graves, como insuficiencia ca^aca congestiva ou perturbapoes dos para-metros quimicos sanguineos.
Caso ainda tenha duvidas sobre a uti-lizapao deste medicamento, fale com o seu medico ou farmaceutico.
4. Efeitos secundarios possiveis_
Como todos os medicamentos, este medicamento pode causar efeitos secundarios, embora estes nao se manifestem em todas as pessoas. Podem ocorrer os seguintes tres efei-tos secundarios relacionados com a utilizapao de Phoxilium:
• volume de agua corporal anormal-mente elevado ou reduzido (hiper ou hipovolemia),
• alterapoes das concentrapoes salinas no sangue (desequilibrio eletrolitico, como hiperfosfate-mia), e
• aumento da concentrapao de bicarbonato no plasma (alcalo-se metabolica) ou redupao da concentrapao de bicarbonato no plasma (acidose metabolica).
Existem tambem alguns efeitos secundarios que podem ser provo-cados por tratamentos de dialise, tais como:
• nauseas, vomitos, caibras mus-culares e pressao arterial baixa (hipotensao).
Comunicapao de efeitos secundarios
Se tiver quaisquer efeitos secundarios, incluindo possiveis efeitos secundarios nao indicados neste folheto, informe o seu medico, far-maceutico ou enfermeiro. Tambem podera comunicar efeitos secunda-rios diretamente ao INFARMED I.P. atraves dos contactos abaixo. INFARMED, I.P.
Direpao de Gestao do Risco de Medicamentos
Parque da Saude de Lisboa, Av. Brasil 53
1749-004 Lisboa
Tel: +351 21 798 73 73
Linha do Medicamento: 800222444
(gratuita)
Fax: + 351 21 798 73 97 Sftio da internet: http://extranet. infarmed.pt/page.seram.frontoffice. seramhomepage
E-mail: farmacovigilancia@infarmed.pt Ao comunicar efeitos secundarios, estara a ajudar a fornecer mais informapoes sobre a seguranpa deste medicamento.
5. Como conservar
Phoxilium_
Manter este medicamento fora da vista e do alcance das crianpas.
Nao utilize este medicamento apos o prazo de validade impresso no rotulo e na embalagem. O prazo de validade corresponde ao ultimo dia do mes indicado.
Conservar entre +4°C e +30°C. Nao refrigerar ou congelar.
A estabilidade quimica e fisica em utilizapao da solupao reconstituida foi demonstrada para 24 horas a +22°C. Se esta nao for imediatamente utilizada, as condipoes e o tempo de armazenamento do produto antes da utilizapao sao da responsabilidade do utilizador, nao devendo ser superior a 24 horas, incluindo a durapao do tratamento.
Nao utilize este medicamento se a solupao estiver turva ou se o involucro exterior estiver danificado. Todos os selos devem estar intactos.
Nao deite fora quaisquer medicamen-tos na canalizapao ou no lixo domes-tico. Pergunte ao seu farmaceutico como deitar fora os medicamentos que ja nao utiliza. Estas medidas ajudarao a proteger o ambiente.
6. Conteudo da embalagem e outras informapoes
to pequeno (A) contem:
Cloreto de calcio, 2 H2O 3,68 g
Cloreto de magnesio, 6 H2O 2,44 g
1000 ml de solupao no compartimen-to grande (B) contem:
Fosfato dissodico, 2 H2O 0,225 g
Substancias ativas apos a mistura:
As solupoes nos compartimentos A (250 ml) e B (4750 ml) sao misturadas para obter uma solupao reconstituida (5000 ml) com a seguinte composipao: mmol/l
Osmolaridade teorica: 293 mOsm/l Os outros componentes sao:
• dioxido de carbono (para ajuste do pH) E290,
• acido cloridrico (para ajuste do pH) E507 e
• agua para preparapoes injetaveis.
Qual o aspeto de Phoxilium e conteudo da embalagem
O Phoxilium e uma solupao para he-modialise e hemofiltrapao apresentada num saco com dois compartimentos.
A solupao final reconstituida e obtida apos a abertura do selo destacavel e subsequente mistura das duas solupoes. A solupao reconstituida e transparente e incolor. Cada saco (A+B) contem 5000 ml de solupao para hemodialise e hemofiltrapao.
O saco e revestido por uma pelicula transparente.
Cada caixa contem dois sacos e um folheto informativo.
Titular da Autoriza9ao de Introdu9ao no Mercado:
Gambro Lundia AB,
Magistratsvagen 16,
SE-226 43 Lund,
SUECIA
Fabricante:
Gambro Dasco S.p.A.
Sondalo Plant,
Via Stelvio 94,
23035 Sondalo (SO),
ITALIA
Este medicamento encontra-se autorizado nos Estados Mem-bros do Espa9o Economico Europeu (EEE) com as seguin-tes denomina9oes:
Austria, Belgica, Bulgaria, Chipre, Di-namarca, Estonia, Finlandia, Franpa, Alemanha, Grecia, Islandia, Irlanda, Italia, Letonia, Lituania, Luxemburgo, Malta, Holanda, Noruega, Polonia, Portugal, Romenia, Eslovaquia, Eslo-venia, Espanha, Suecia, Reino Unido: Phoxilium
Hungria: Phoxil
Este folheto foi revisto pela ultima vez em 05/2015
PHOXILIUM 1,2 mmol/l de fosfato
Solucion para hemodialisis y hemofiltracion
Cloruro de calcio dihidratado, cloruro de magnesio hexahidratado, cloruro de sodio, bicarbonato de sodio, cloruro de potasio, fosfato disodico dihidratado.
Lea todo el prospecto detenidamente antes de empezar a usar este medicamento, porque contiene informacion importante para usted.
• Conserve este prospecto, ya que puede tener que volver a leerlo.
• Si tiene alguna duda, consulte a su medico, farmaceutico o enfermero.
• Si experimenta efectos adversos, consulte a su medico, farmaceutico o enfermero, incluso si se trata de efectos adversos que no aparecen en este prospecto. Ver seccion 4.
Contenido del prospecto
1. Que es PHOXILIUM y para que se utiliza
2. Que necesita saber antes de recibir PHOXILIUM
3. Como usar PHOXILIUM
4. Posibles efectos adversos
5. Conservacion de PHOXILIUM
6. Contenido del envase e informacion adicional
1. Que es PHOXILIUM y para que se utiliza_
PHOXILIUM, que pertenece al grupo de soluciones de hemofiltrados, contiene cloruro de calcio dihidratado, cloruro de magnesio hexahidratado, cloruro de sodio, bicarbonato de sodio, cloruro de potasio y fosfato disodico dihidratado.
PHOXILIUM se utiliza en hospitales en tratamientos de cuidados intensivos para corregir el desequilibrio quimico causado por una lesion renal.
El objetivo de estos tratamientos, que incluyen terapia de sustitucion renal, es eliminar de la sangre los productos de desecho que se acumulan cuando los rinones no funcionan bien.
La solucion PHOXILIUM se utiliza especialmente en el tratamiento de pacientes en estado critico con una lesion renal aguda y que ademas presentan:
• una concentracion normal de potasio en sangre (caliemia normal), o bien
• una concentracion normal o baja de fosfato en sangre (fosfatemia normal o hipofosfatemia).
2. Que necesita saber antes de recibir PHOXILIUM_
No utilizar PHOXILIUM en pacientes que presenten alguna de las tres condiciones siguientes:
• una concentracion alta de potasio en sangre (hipercaliemia)
• una concentracion alta de bicarbonato en sangre (alcalosis metabolica)
• una concentracion alta de fosfato en sangre (hiperfosfatemia)
No someter al paciente a hemodialisis ni hemofiltracion en los tres casos descritos a continuacion:
• Si la hemofiltracion no puede corregir los sintomas causados por una concentracion elevada de urea en sangre (sintomas uremicos) como consecuencia de una lesion renal con hipercatabolismo acusado (un aumento anormal del proceso de degradacion de sustancias).
• Si la presion arterial en el acceso vascular es insuficiente.
• Si la capacidad de coagulacion sanguinea es reducida (anticoagulacion sistemica) y existe riesgo elevado de que se produzca una hemorragia.
Advertencias y precauciones
Consulte a su medico, farmaceutico o enfermero antes de empezar a usar PHOXILIUM.
La condicion de su sangre se comprobara antes y durante el tratamiento. Se controlara, por ejemplo, el equilibrio acidobasico y la concentracion de sales en la sangre (electrolitos), incluidas todas las entradas (perfusion intravenosa) y salidas (diuresis) de liquidos, incluso las que no esten relacionadas directamente con el tratamiento TCRR.
Uso de PHOXILIUM con otros medicamentos
Comunique a su medico o farmaceutico si esta utilizando, ha utilizado recientemente o podria tener que utilizar cualquier otro medicamento. Debe hacerlo porque la concentracion de algunos medicamentos puede afectar durante el tratamiento con PHOXILIUM. Su medico decidira si es preciso modificar la dosis de los medicamentos que utiliza.
En concreto, hable con su medico si toma alguno de los medicamentos siguientes:
• Suplementos de fosfato (por ejemplo, liquidos nutritivos), ya que pueden aumentar el riesgo de concentracion alta de fosfato en sangre (hiperfosfatemia).
• Vitamina D y medicamentos que contengan cloruro de calcio o gluconato de calcio, ya que pueden aumentar el riesgo de concentracion alta de calcio en sangre (hipercalcemia).
• Bicarbonato de sodio, ya que puede provocar un aumento del riesgo de que exista exceso de bases en la sangre (alcalosis metabolica).
Embarazo, lactancia y fertilidad
Embarazo y lactancia:
No hay datos clinicos documentados sobre el uso de este medicamento durante el embarazo y la lactancia. Este medicamento solo debe administrarse a mujeres embarazadas y en periodo de lactancia si es claramente necesario.
5. Conservacion de
PHOXILIUM_
Mantener este medicamento fuera de la vista y del alcance de los ninos.
No utilice este medicamento despues de la fecha de caducidad que aparece en la etiqueta y en el envase. La fecha de caducidad es el ultimo dia del mes que se indica. Conservar a una temperatura entre +4°C y +30°C. No refrigerar o congelar.
Se ha demostrado la estabilidad fisica y quimica en uso de la solucion reconstituida durante 24 horas a 22°C. De no utilizar la solucion inmediatamente, las condiciones y el tiempo de almacenamiento seran responsabilidad del usuario; en cualquier caso, este tiempo no debe ser superior a 24 horas, incluida la duracion del tratamiento. No utilizar este medicamento si la solucion esta turbia o si el envoltorio presenta algun dano. Todos los precintos deben estar intactos.
Los medicamentos no se deben tirar por los desagues ni a la basura. Pregunte a su farmaceutico como deshacerse de los envases y de los medicamentos que ya no necesita. De esta forma, ayudara a proteger el medio ambiente.
Fertilidad:
No se preve ningun efecto en la fertilidad, dado que el calcio, el sodio, el potasio, el magnesio, el cloruro, el hidrogenofosfato y el bicarbonato son componentes normales del organismo.
Conduccion y uso de maquinas
PHOXILIUM no afecta a la capacidad para conducir vehiculos o manejar maquinaria.
3. Como usar PHOXILIUM
PHOXILIUM es un producto de uso hospitalario que solo debe ser administrado por profesionales medicos. El volumen de PHOXILIUM empleado y, por lo tanto, la dosis, dependera de sus condiciones. El volumen de dosis sera determinado por el medico responsable del tratamiento. PHOXILIUM puede administrate directamente en la corriente sanguinea (via intravenosa) o mediante hemodialisis, una tecnica en la que la solucion circula por un lado de la membrana de dialisis mientras la sangre lo hace por el otro.
Siga exactamente las instrucciones de administracion del medicamento contenidas en este prospecto o las indicadas por su medico, farmaceutico o enfermero. En caso de duda, pregunte a su medico, farmaceutico o enfermero.
Para obtener instrucciones de uso, consulte el apartado “Esta informacion esta destinada unicamente a profesionales del sector sanitario”.
Si usa mas PHOXILIUM del que debe
PHOXILIUM es un producto de uso hospitalario que es administrado unicamente por profesionales medicos; ademas, se lleva a cabo un control exhaustivo del equilibrio de liquidos, asi como analiticas sangumeas.
Por lo tanto, es improbable que use mas PHOXILIUM del que debe.
En el caso improbable de que se produzca una sobredosis, el medico adoptara las medidas correctivas necesarias y ajustara la dosis.
La sobredosis puede derivar en una sobrecarga de liquidos, en una reduccion de la concentracion de bicarbonato en el plasma (acidosis metabolica) o en una concentracion elevada de fosfato (hiperfosfatemia) si el paciente tiene una lesion renal.
Podria tener consecuencias muy graves, como insuficiencia cardiaca congestiva o alteraciones del equilibrio acido-basico o electrolitico.
Si tiene cualquier otra duda sobre el uso de este medicamento, pregunte a su medico o farmaceutico.
4. Posibles efectos
adversos_
Al igual que todos los medicamentos, este medicamento puede producir efectos adversos, aunque no todos las personas los sufran.
Es posible que el paciente experimente los tres efectos secundarios relacionados con el uso de PHOXILIUM que se describen a continuacion:
• Volumen de agua en el cuerpo anormalmente elevado o reducido (hiper o hipovolemia)
• Variaciones en los niveles de sales en la sangre (desequilibrios electroliticos, como hiperfosfatemia)
• Aumento de la concentracion de bicarbonato en el plasma (alcalosis metabolica) o reduccion de la concentracion de bicarbonato en el plasma (acidosis metabolica)
Existen ademas algunos efectos secundarios que pueden deberse a los tratamientos de dialisis, por ejemplo:
• Nauseas, vomitos, calambres musculares y presion arterial baja (hipotension).
Comunicacion de efectos adversos
Si experimenta cualquier tipo de efecto adverso, consulte a su medico, farmaceutico o enfermero, incluso si se trata de posibles efectos adversos que no aparecen en este prospecto. Tambien puede comunicarlos directamente a traves del Sistema Espanol de Farmacovigilancia de
Medicamentos de Uso Humano: www.notificaRAM.es. Mediante la comunicacion de efectos adversos usted puede contribuir a proporcionar mas informacion sobre la seguridad de este medicamento.
6. Contenido del envase e informacion adicional
Composicion de PHOXILIUM
A continuacion se enumeran los principios activos antes y despues de la mezcla (reconstitucion) de la solucion.
Los principios activos antes de la mezcla son:
1,000 ml de solucion del compartimento pequeno (A)
contienen:
Cloruro de calcio, 2 H2O 3,68 g
Cloruro de magnesio, 6 H2O 2,44 g
1.000 ml de solucion del compartimento grande (B)
contienen:
Fosfato disodico, 2 H2O 0,225 g
Los principios activos despues de la mezcla son:
Las soluciones de los compartimentos A (250 ml) y B (4.750 ml) se mezclan para producir una solucion reconstituida (5.000 ml) cuya composicion es la siguiente:
mmol/l
Osmolaridad teorica: 293 mOsm/l Los demas componentes son:
• Dioxido de carbono (para ajuste de pH) E290
• Acido clorhidrico (para ajuste de pH) E507
• Agua para preparaciones inyectables
Aspecto del producto y contenido del envase
PHOXILIUM es una solucion para hemodialisis y hemofiltracion que se presenta en una bolsa que consta de dos compartimentos.
La solucion final reconstituida se obtiene tras romper el sello hermetico y mezclar ambas soluciones. La solucion reconstituida es transparente e incolora. Cada bolsa (A+B) contiene 5.000 ml de solucion para hemodialisis y hemofiltracion. La bolsa esta envuelta en pelicula transparente.
Cada caja contiene dos bolsas y un prospecto.
Titular de la autorizacion de comercializacion y responsable de la fabricacion:
Gambro Lundia AB Magistratsvagen 16 SE-226 43 Lund SUECIA
Fabricante:
Gambro Dasco S.p.A Sondalo Plant, Via Stelvio 94, 23035 Sondalo (SO)
ITALIA
Pueden solicitar mas informacion respecto a este medicamento dirigiendose al representante local del titular de la autorizacion de comercializacion:
Baxter, S.L.,
Poligono industrial sector 14,
C/ Pouet de Camilo n°2,
46394 Ribarroja del Turia,
Valencia,
Espana
Este medicamento esta autorizado en los estados miembros del Espacio Economico Europeo con los siguientes nombres:
Alemania, Austria, Belgica, Bulgaria, Chipre, Dinamarca, Eslovaquia, Eslovenia, Espana, Estonia, Finlandia, Francia, Grecia, Islandia, Irlanda, Italia, Letonia, Lituania, Luxemburgo, Malta, Noruega, Paises Bajos, Polonia, Portugal, Reino Unido, Rumania y Suecia: PHOXILIUM
Hungria: PHOXIL
Fecha de la ultima revision de este prospecto: 07/2016
La informacion detallada y actualizada de este medicamento esta disponible en la pagina Web de la Agencia Espanola de Medicamentos y Productos Sanitarios (AEMPS) http://www. aemps.es
PHOXILIUM 1.2 mmol/l phosphate
Solution for haemodialysis and haemofiltration
The instructions for use / Handling for PHOXILIUM must be strictly followed.
The solutions in the two compartments must be mixed before use. Use of a contaminated solution may cause sepsis and shock. PHOXILIUM may be warmed to 37°C to enhance patient comfort. However, only dry heat should be used. Solutions should not be heated in water or in a microwave oven. PHOXILIUM should be inspected visually for particulate matter and discoloration prior to administration. Do not administer unless the solution is clear and the seal is intact.
The inorganic phosphate concentration should be measured regularly. Inorganic phosphate must be substituted in cases of low level of phosphate in the blood.
Additional sodium bicarbonate substitution may increase the risk of metabolic alkalosis.
The volume and rate at which PHOXILIUM is administered depends on the blood concentration of phosphate and other electrolytes, acid-base balance, and overall clinical condition of the patient. Administration (dose, infusion rate and cumulative volume) of PHOXILIUM should be established by a physician. Continued application of haemofiltration will remove excess fluid and electrolytes.
In case of fluid imbalance, the clinical situation must be carefully monitored and fluid balance must be restored:
• In case of hypervolaemia, the net ultrafiltration rate prescribed for the CRRT device can be increased and/or the rate of administration of solutions other than replacement fluid and/or dialysate can be reduced.
• In case of hypovolemia, the net ultrafiltration rate prescribed for the CRRT device can be reduced and/or the rate of administration of solutions other than replacement fluid balance and/ or dialysate can be increased.
Because PHOXILIUM is a potassium-containing solution, hyperkalemia may occur transiently after treatment is initiated. Decrease the infusion rate and confirm that the desired potassium concentration is achieved. If hyperkalemia does not resolve, stop administration promptly.
Because PHOXILIUM is a phosphate-containing solution, hyperphosphatemia may occur transiently after treatment is initiated. The infusion rate shall be decreased until the desired phosphate concentration is achieved.
If hyperphosphatemia does not resolve, the administration shall be stopped promptly.
Electrolyte and blood acid-base parameters should be monitored regularly in patients treated with PHOXILIUM. PHOXILIUM contains hydrogen phosphate, a weak acid that can influence the patient's acid-base balance. If metabolic acidosis develops or worsens during therapy with PHOXILIUM, the infusion rate may need to be decreased or its administration stopped.
The range of flow rates for the replacement solution in haemofiltration and haemodiafiltration are: Adult and
adolescents: 500 - 3000 ml/h
Children: 15 - 35 ml/kg/h
The range of flow rates for the dialysate in continuous haemodialysis and continuous haemodiafiltra-tion are:
Adult and
adolescents: 500 - 2500 ml/h
Children: 15 - 30 ml/kg/h
INSTRUCTION FOR USE / HANDLING
The solution in the small compartment A is added to the solution in the large compartment B after breaking the peel seal immediately before use. The reconstituted solution shall be clear and colourless. Aseptic technique shall be used throughout the handling and administration to the patient.
Use only if the overwrap is undamaged, all seals are intact, peel seal is not broken, and the solution is clear. Press bag firmly to test for any leakage. If leakage is discovered, discard the solution immediately since sterility can no longer be assured.
The large compartment B is fitted with an injection port for the possible addition of other necessary drugs after reconstitution of the solution. It is the responsibility of the user to judge the compatibility of an additive medication with PHOXILIUM by checking for eventual colour change and/or eventual precipitation, insoluble complexes or crystals. Before adding a medication, verify if it is soluble and stable in this medicine and that the pH range of PHOXILIUM is appropriate (pH of reconstituted solution is 7.0-8.5). Additives may be incompatible. The Instructions for Use of the medication to be added must be consulted.
Remove any fluid from the injection port, hold the bag upside down, insert the drug through the injection port and mix thoroughly. The solution must be administered immediately.
X...............................................................................................................................................................................................................................................................................................................................X
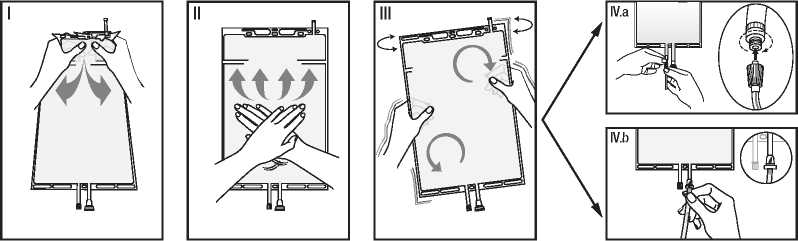
I Remove the overwrap from the bag immediately before use and discard any other packaging materials. Open the seal by holding the small compartment with both hands and squeeze it until an opening is created in the peel seal between the two compartments.
(See figure I below)
II Push with both hands on the large compartment until the peel seal between the two compartments is entirely open. (See figure II below)
III Secure complete mixing of the solution by shaking the bag gently. The solution is now ready for use, and can be hung on the equipment.
(See figure III below)
IV The dialysis or replacement line may be connected to either of the two access ports.
IV.a If the luer access is used, remove the cap with a twist and pull motion, and connect the male luer lock on the dialysis or replacement line to the female luer receptor on the bag using a push and twist motion. Ensure that the connection is fully seated and tighten. The connector is now open. Verify that the fluid is flowing freely.
(See figure IV.a below)
When the dialysis or replacement line is disconnected from the luer connector, the connector will close and the flow of the solution will stop. The luer port is a needle-less and swabbable port.
IV.b If the injection port is used, first remove the snap-off cap. Then introduce the spike through the rubber septum. Verify that the fluid is flowing freely.
(See figure IV.b below)
The reconstituted solution should be used immediately. If not used immediately, the reconstituted solution should be used within 24 hours, including the duration of the treatment, after addition of solution A to solution B.
The reconstituted solution is for single use only. Discard any unused solution immediately after use.
Any unused medicinal product or waste material should be disposed of in accordance with local requirements.
A informagao que se segue destina-se apenas aos profissionais de saude
PT
Phoxilium 1,2 mmol/l fosfato Solugao para hemodialise ou hemofiltragao
As instrugoes de Utilizagao/Manu-seamento do Phoxilium devem ser cuidadosamente seguidas.
As solugoes dos dois compartimen-tos tem de ser misturadas antes da utilizagao.
A utilizagao de uma solugao contaminada pode causar sepsis e choque.
O Phoxilium pode ser aquecido a +37°C para aumentar o conforto do doente. No entanto, apenas deve ser utilizado calor seco. As solugoes nao devem ser aquecidas em agua ou no micro-ondas.
O Phoxilium deve ser inspecionado visualmente para a detegao de particulas em suspensao e desco-loragao antes da administragao. Nao administrar a nao ser que a solugao esteja limpida e que o selo esteja intacto.
A concentragao de fosfatos inorga-nicos deve ser medida com regula-ridade. O fosfato inorganico tem de ser substituido nos casos de baixo nivel de fosfato no sangue.
A substituigao adicional de bicar-bonato de sodio pode aumentar o risco de alcalose metabolica.
O volume e taxa de Phoxilium administrado depende da concentragao de fosfato e outros eletrolitos no sangue, do equilibrio acido-base e da condigao clinica geral do doente. A administragao (dose, taxa de perfusao e volume cumulativo) de Phoxilium deve ser determinada por um medico. A apli-cagao contmua de hemofiltragao ira remover o excesso de liquidos e de eletrolitos.
No caso de desequilibrio hidrico, a condigao clinica tem de ser cuida-dosamente monitorizada tendo o equilibrio hidrico de ser reposto:
• Em caso de hipervolemia, a taxa liquida de ultrafiltragao prescrita para o dispositivo CRRT pode ser aumentada e/ ou a taxa de administragao de outras solugoes para alem do
fluido de reposigao e/ou diali-sante pode ser reduzida.
• Em caso de hipovolemia, a taxa liquida de ultrafiltragao prescrita para o dispositivo CRRT pode ser reduzida e/ou a taxa de ad-ministragao de outras solugoes para alem do equilibrio de fluido de reposigao e/ou dialisante pode ser aumentada.
Uma vez que Phoxilium e uma solugao que contem potassio, pode ocorrer hipercalemia transitoria apos o inicio do tratamento. Dimi-nua a taxa de perfusao e confirme que a concentragao desejada de potassio e alcangada. Se a hiper-calemia nao for resolvida, interrom-pa a administragao de imediato. Uma vez que Phoxilium e uma solugao que contem fosfato, pode ocorrer hiperfosfatemia transitoria apos o inicio do tratamento. A taxa de perfusao deve ser reduzida ate que se atinja a concentragao de fosfato pretendida. Se a hiperfos-fatemia nao for resolvida, a admi-nistragao deve ser interrompida de imediato.
Os parametros sanguineos de eletrolitos e de acido-base devem ser monitorizados regularmente em doentes tratados com Phoxilium. Phoxilium contem hidrogenofos-fato, um acido fraco que pode influenciar o equilibrio acido/base do doente. Se se desenvolver acidose metabolica ou esta piorar durante a terapia com Phoxilium, a taxa de perfusao podera ter de ser reduzida ou a administragao interrompida.
Os intervalos das taxas de fluxo para a solugao de substituigao na hemofiltragao e hemodiafiltragao sao os seguintes:
Adultos e
adolescentes: 500 - 3000 ml/h
Criangas: 15 - 35 ml/kg/h
Os intervalos das taxas de fluxo para o dialisado na hemodialise e hemodiafiltragao continuas sao os seguintes Adultos e
adolescentes: 500 - 2500 ml/h
Criangas: 15 - 30 ml/kg/h
Instrugoes de utilizagao e manuseamento
A solugao do compartimento pequeno A e adicionada a solugao do compartimento grande B apos partir o selo autocolante, ime-diatamente antes da utilizagao.
A solugao reconstituida deve ser limpida e incolor.
A tecnica assetica deve ser utili-zada durante todo o periodo de manuseamento e administragao ao doente.
Utilize apenas se o involucro exterior estiver intacto, se todos os selos estiverem intactos, se o selo autocolante nao estiver partido e se a solugao estiver limpida. Pressione firmemente o saco para verificar a existencia de fugas. Se for detetada uma fuga, rejeite a solugao imediatamente uma vez que a sua esterilidade ja nao pode ser garantida. O compartimento grande B tem uma porta de injegao para a possivel adigao de outros medicamentos necessarios apos a reconstituigao da solugao. £ da responsabilidade do utilizador a avaliagao da medicagao aditiva com Phoxilium por verificacao da eventual alteragao da cor e/ou eventual precipitagao, formagao de complexos insoluveis ou cristais. Antes de adicionar uma subs-tancia ou medicagao, verifique se e soluvel e/ou estavel no pH do Phoxilium (o pH da solugao reconstituida e de 7,0 - 8,5). Os aditivos podem ser incompativeis. As instrugoes de utilizagao da medicagao a ser adicionada devem ser consultadas.
So se deve adicionar medicamen-tos a solugao, sob a responsabili-dade de um medico, da seguinte forma:
Remova qualquer residuo de liqui-do da porta de injegao, segure o saco voltado para baixo, introduza o farmaco atraves da porta de in-jegao e misture completamente. A solugao devera ser administrada imediatamente.
K...............................................................................................................................................................................................................................................................................................................................X
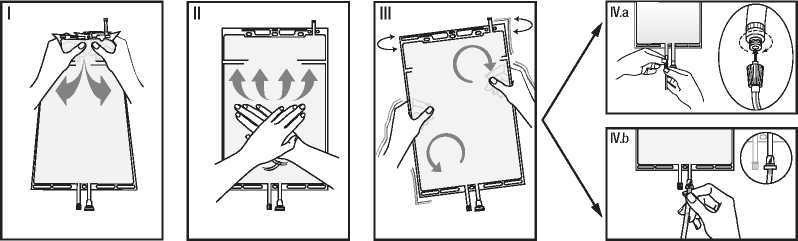
I Remova o involucro exterior do saco imediatamente antes da utilizagao e elimine quaisquer outros materiais de embala-gem. Abra o selo, segurando o compartimento pequeno com as duas maos e apertando-o ate criar uma abertura no selo destacavel entre os dois com-partimentos. (Consulte a figura I abaixo)
II Pressione o compartimento grande com as duas maos ate que o selo destacavel entre os dois compartimentos esteja completamente aberto. (Consulte a figura II abaixo)
III Agite o saco suavemente para assegurar a mistura completa da solugao. A solugao esta agora pronta a ser utilizada e pode ser suspensa no equipa-mento. (Consulte a figura III abaixo)
IV A linha de dialise ou de substi-tuigao pode ser ligada a qual-quer uma das duas portas de acesso.
IV.a Se estiver a ser utilizado o acesso luer, remova a tampa, rodando e puxando, e ligue o luer lock macho na linha de di-alise ou de reposigao ao rece-tor luer femea no saco, empur-rando e rodando. Certifique-se de que ficam bem ligados. Desta forma, o conector fica aberto. Verifique se a solugao flui livremente. (Consulte a figura IV.a abaixo)
Quando a linha de dialise ou de reposigao e separada do conector luer, o conector fecha e a solugao deixa de fluir. A porta luer e uma porta sem agulha e lavavel.
IV.b Se estiver a ser utilizada a porta de injegao, em primeiro lu-gar, retire a tampa. De seguida, introduza o espigao atraves do septo de borracha. Verifique se a solugao flui livremente. (Consulte a figura IV.b abaixo)
A solugao reconstituida deve ser utilizada imediatamente. Caso nao o seja, a solugao reconstitu-Ida deve ser utilizada no prazo de 24 horas, incluindo a duragao do tratamento, apos a adigao da solugao A a solugao B.
A solugao reconstituida destina-se a uma unica utilizagao. Elimine imediatamente apos utilizagao, qualquer porgao nao utilizada da solugao.
Qualquer medicamento nao utilizado ou residuos devem ser eliminados de acordo com as exi-gencias locais.
Esta informacion esta destinada unicamente a profesionales del sector sanitario
ES
PHOXILIUM 1,2 mmol/l de fosfato
Solucion para hemodialisis y hemofiltracion
Debe seguir con exactitud las instrucciones de uso y manipulacion de PHOXILIUM.
Las soluciones de los dos compartimentos deben mezclarse antes de usarse.
El uso de una solucion contaminada puede causar sepsis y shock.
Para aumentar la comodidad del paciente, se puede calentar PHOXILIUM hasta alcanzar los 37°C. No obstante, solo debe utilizarse calor seco. Las soluciones no se deben calentar en agua ni en un horno microondas. Antes de la administracion, se debe comprobar visualmente que PHOXILIUM no contenga particulas ni haya perdido el color original. No administre la solucion a menos que esta sea transparente y el precinto este intacto.
La concentracion de fosfato inorganico debe determinarse periodicamente. El fosfato inorganico debe sustituirse en aquellos casos en los que el nivel de fosfato en sangre sea bajo.
La adicion de bicarbonato sodico de sustitucion puede aumentar el riesgo de alcalosis metabolica.
El volumen y la velocidad a la que se administra PHOXILIUM dependen de la concentracion de fosfato y otros electrolitos en la sangre, del equilibrio acido-basico y del estado clinico general del paciente. La pauta de administracion (dosis, velocidad de la perfusion y volumen acumulado) de PHOXILIUM debera determinarla un medico.
La aplicacion continuada de hemofiltracion eliminara el exceso de liquidos y electrolitos.
En caso de desequilibrio de liquidos, se debe supervisar minuciosamente la situacion clinica y restaurar el equilibro de liquidos:
• En caso de hipervolemia, la velocidad de la ultrafiltracion
neta prescrita para el dispositivo de TCRR puede aumentarse y la velocidad de administracion de aquellas soluciones distintas de los liquidos de rehidratacion y el liquido de dialisis puede reducirse.
• En caso de hipovolemia, la velocidad de la ultrafiltracion neta prescrita para el dispositivo de TCRR puede reducirse y la velocidad de administracion de aquellas soluciones distintas de los liquidos de rehidratacion y el liquido de dialisis puede aumentarse.
PHOXILIUM es una solucion que contiene potasio, por lo que puede provocar hipercaliemia transitoria durante el tratamiento. En tal caso, reduzca la velocidad de perfusion y asegurese de que se haya alcanzado la concentracion de potasio necesaria. Si la hipercaliemia no remite, suspenda el tratamiento de inmediato.
Debido a que PHOXILIUM es una solucion que contiene fosfato, puede provocar hiperfosfatemia temporal una vez iniciado el tratamiento. En tal caso, se debe reducir la velocidad de perfusion hasta alcanzar la concentracion de fosfato deseada. Si la hiperfosfatemia no remite, la administracion debe suspenderse de inmediato.
Los electrolitos y los parametros acido-basicos en sangre deben controlarse periodicamente en los pacientes tratados con PHOXILIUM. PHOXILIUM contiene bifosfato, un acido debil que puede afectar al equilibrio acidobasico del paciente. Si durante el tratamiento con PHOXILIUM aparece acidosis metabolica o esta empeora, es posible que sea necesario reducir la velocidad de perfusion o suspender la administracion.
La velocidad de flujo de la solucion de sustitucion en terapias de hemofiltracion y hemodiafiltracion es:
Adultos y
adolescentes: 500 - 3.000 ml/h
Ninos: 15 - 35 ml/kg/h
La velocidad de flujo del Kquido de dialisis en terapias de hemodialisis y hemodiafiltracion continua es: Adultos y
adolescentes: 500 - 2.500 ml/h
Ninos: 15 - 30 ml/kg/h
Instrucciones de uso y manipulacion
La solucion del compartimento pequeno A se anade a la solucion del compartimento grande B tras romper el vastago rompible o el precinto e inmediatamente antes utilizarse. La solucion reconstituida debe ser transparente e incolora.
Se debe emplear una tecnica aseptica durante la manipulacion y administracion al paciente.
Utilizar solamente si el envoltorio esta mtegro, los precintos estan intactos, el sello despegable no esta roto y la solucion es transparente. Apriete la bolsa para asegurarse de que no haya fugas. Si se descubre alguna fuga, deseche la solucion inmediatamente ya que no se puede garantizar su esterilidad.
El compartimento grande B tiene un acceso de inyeccion para anadir otros farmacos que sean necesarios una vez reconstituida la solucion. Es responsabilidad del medico juzgar la compatibilidad de la medicacion anadida a la solucion PHOXILIUM comprobando el cambio evantual de color y/o precipitacion, complejos insolubles o cristales. Antes de anadir un medicamento, compruebe que sea soluble y estable en agua en el intervalo de pH de PHOXILIUM (el intervalo de pH de la solucion reconstituida es 7,0-8,5).
Los aditivos podrian no ser compatibles. Se deben consultar las instrucciones de uso del medicamento que se va a anadir. Retire cualquier liquido del acceso de inyeccion, sujete la bolsa en posicion vertical hacia abajo, anada el farmaco a traves del puerto de inyeccion y mezcle completamente.
La solucion debe administrarse inmediatamente.
X...............................................................................................................................................................................................................................................................................................................................X
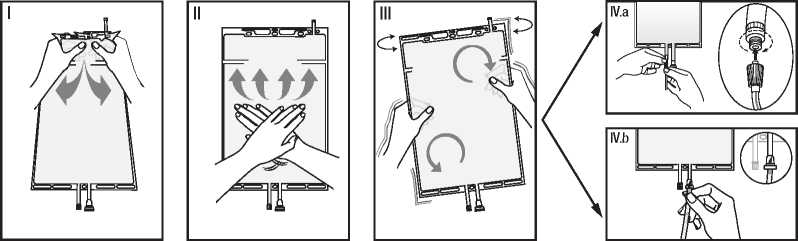
I Retire el envoltorio de la bolsa inmediatamente antes de usarla y deseche los demas materiales de embalaje.
Rompa el sello hermetico sujetando el compartimento pequeno entre las dos manos y apretando hasta que se abra la pared que separa ambos compartimentos (vea la figura I que aparece abajo).
II Presione el compartimento grande con ambas manos hasta que la pared entre los dos compartimentos este totalmente abierta (vea la figura II que aparece abajo).
III Asegurese de que las soluciones se mezclan completamente agitando la bolsa suavemente. La solucion ya esta lista para su uso y la bolsa puede colgarse en el equipo (vea la figura III que parece abajo).
IV La linea de dialisis o de
sustitucion puede conectarse a cualquiera de los dos conectores de acceso.
IV.a Si se utiliza el conector luer, quite el tapon y conecte el conector luer macho de la linea de dialisis o sustitucion en el receptor luer hembra de la bolsa mediante un movimiento de presion y giro. Asegurese de que la conexion esta bien hecha y apretada. La conexion se abrira. Compruebe que el Kquido circula libremente. (vea la figura IV.a que aparece abajo).
Si la linea de dialisis o sustitucion se desconecta del conector luer, el conector se cerrara y el flujo de la solucion se detendra. El puerto luer es un puerto sin aguja que se puede limpiar.
IV.b Si se utiliza el acceso de
inyeccion, retire antes el tapon levantandolo. Introduzca despues el espigon a traves de la pared de goma. Compruebe que el liquido circula libremente (vea la figura IV.b que aparece abajo)
La solucion reconstituida debe utilizarse inmediatamente. En caso de no utilizarla inmediatamente, tenga en cuenta que la solucion reconstituida debe utilizarse en el plazo de las 24 horas posteriores a la adicion de la solucion A a la solucion B, incluida la duracion del tratamiento.
La solucion reconstituida es para un solo uso. Deseche la solucion sobrante inmediatamente despues del uso.
La eliminacion del medicamento no utilizado y de todos los materiales que hayan estado en contacto con el, se realizara de acuerdo con la normativa local.
THIS PAGE IS INTENTIONALLY LEFT BLANK
THIS PAGE IS INTENTIONALLY LEFT BLANK

Gambro and Phoxilium are trademarks of Baxter International Inc., or its subsidiaries


CD
<
2 o
_Q CD
I O
O CL